Liste des codes intra GHS : comprendre comment ça fonctionne
22 mars 2022

A partir du mois d’avril 2022, une nouvelle liste de dispositifs médicaux fera l’objet d’un regard particulier de la part des autorités de tutelle. Les établissements de santé devront fournir auprès de l’ATIH le détail de l’utilisation de ces dispositifs dans un fichier complémentaire au fichier T2A. Nous vous proposons donc dans cet article un éclairage sur les dispositifs inscrits sur la liste intra-GHS.
Comment sont financés les dispositifs médicaux dans les hôpitaux et les cliniques ?
Les dispositifs médicaux (DM) utilisés en établissement de santé sont financés très généralement par une enveloppe globale dans les Groupes Homogènes de Séjour (GHS).
En clair et de façon simplifiée, lorsqu’un patient vient à l’hôpital on pose un diagnostic lié à sa pathologie, ce diagnostic donne un GHS et ce GHS correspond à un montant remboursé à l’établissement pour prendre en charge ce malade. Dans ce tarif de prise en charge est inclus le remboursement de la majorité des DM.
Néanmoins, certains DM à usage individuel utilisés en établissement de santé et ne pouvant être intégrés dans les GHS sont financés en supplément (hors-GHS). Ces dispositifs sont inscrits sur la liste en sus, et donc sur la liste des produits et des prestations remboursables (LPPR). Cette inscription se fait après avis de la CNEDIMTS, sur recommandation du Conseil de l’Hospitalisation et par décision du ministre de la Santé prise par arrêté.
Enfin, et c’est le sujet de cet article, certains DM financés dans le GHS doivent être inscrits sur une liste positive dite « liste intra-GHS ». Ces DM ne pourront être achetés, fournis, pris en charge et utilisés par les établissements de santé que s’ils sont sur cette liste.
Quels sont les dispositifs inscrits sur la liste intra-GHS ?
Sont inscrits sur la liste intra-GHS les dispositifs médicaux à caractère invasif ou présentant des risques pour la santé humaine.
Les dispositifs sont répartis dans 10 classes différentes, on parle de catégorie homogène intra-GHS.
Les catégories homogènes intra-GHS sont les suivantes :
- les défibrillateurs cardiaques implantables conventionnels avec sonde endocavitaire (simple, double et triple chambre) ;
- les défibrillateurs cardiaques implantables sans sonde endocavitaire ;
- les stents intracrâniens utilisés dans l’angioplastie des sténoses athéromateuses ;
- les valves cardiaques chirurgicales biologiques avec suture
- les valves cardiaques chirurgicales biologiques sans suture
- les dispositifs implantables destinés au traitement par voie vaginale du prolapsus des organes pelviens ;
- les dispositifs implantables destinés au traitement par voie vaginale de l’incontinence urinaire ;
- les dispositifs destinés au traitement par voie haute du prolapsus des organes pelviens ;
- les stents intracrâniens pour diversion de flux (flow diverter) ;
- les dispositifs de thrombectomie, comprenant les stents retrievers, les systèmes de thrombo-aspiration ainsi que les cathéters guide à ballonnets spécifiques à la thrombectomie.
Les arrêtés qui officialisent ces 10 catégories sont les suivants : arrêté du 28 novembre 2013, arrêtés du 26 novembre 2019 et du 28 mai 2020, du 23 septembre 2020 et du 20 février 2021.
Les dispositifs concernés sont classés dans les catégories homogènes intra-GHS. Voici quelques exemples :
- Le dispositif EMBLEM S-ICD (modèle A 219) de la société Cardiac Pacemakers Incorporated est inscrit dans la catégorie « Défibrillateur cardiaque implantable sans sonde endocavitaire ».
- Le dispositif CYRENE de la société Anlytic Biosurgical Solutions est inscrit dans la catégorie « Dispositifs implantables destinés au traitement par voie vaginale de l’incontinence urinaire »
La liste complète est disponible sur le site du ministère de la santé.
C’est quoi un code intra-GHS ?
Un code intra GHS est un code attribué à un groupe de dispositifs médicaux s’il est inscrit en ligne générique ou à un dispositif médical particulier s’il est inscrit en nom de marque.
Seule la catégorie homogène intra-GHS « défibrillateurs cardiaques implantables conventionnels avec sonde endocavitaire (simple, double et triple chambre) » comporte des dispositifs inscrits en ligne générique. Les autres catégories comportent exclusivement des dispositifs inscrits en nom de marque.
Les catégories homogènes intra-GHS sont découpées en sous-groupes.
Prenons quelques exemples pour une inscription en ligne générique.
La catégorie homogène intra-GHS « défibrillateurs cardiaques implantables conventionnels avec sonde endocavitaire » est découpée en 3 sous-sections, à chaque sous-section est attribué un code intra-GHS :
- les « défibrillateurs cardiaques implantables conventionnels avec sonde endocavitaire simple chambre » ont le code intra GHS est le DAI001.
- les « défibrillateurs cardiaques implantables conventionnels avec sonde endocavitaire double chambre » ont le code intra GHS est le DAI002.
- les « défibrillateurs cardiaques implantables conventionnels avec sonde endocavitaire triple chambre » ont le code intra GHS est le DAI003.
Pour une inscription en nom de marque c’est chaque dispositif qui dispose de son propre code intra-GHS.
Nous pouvons prendre pour exemple la catégorie homogène intra-GHS « valve cardiaque chirurgicales biologiques avec sutures », cette catégorie est découpée en 3 sous-sections, chaque sous-section comporte des dispositifs médicaux inscrits en nom de marque.
Sous-section 1 : Bioprothèses valvulaires aortiques
- CROWN PRT, Bioprothèse valvulaire aortique avec armature Code : BVA001
- SOLO SMART, Bioprothèse valvulaire aortique sans armature Code : BVA002
- EPIC, Bioprothèse valvulaire aortique avec armature Code : BVA003
- EPIC SUPRA, Bioprothèse valvulaire aortique avec armature Code : BVA004
- TRIFECTA, Bioprothèse valvulaire aortique avec armature Code : BVA005
- TRIFECTA GT, Bioprothèse valvulaire aortique avec armature Code : BVA006
- HANCOCK II, Bioprothèse valvulaire aortique avec armature Code : BVA007
- HANCOCK II ULTRA, Bioprothèse valvulaire aortique avec armature Code : BVA008
- MOSAIC, Bioprothèse valvulaire aortique avec armature Code : BVA009
- MOSAIC ULTRA, Bioprothèse valvulaire aortique avec armature Code : BVA010
- PRESTYLED FREESTYLE, Bioprothèse valvulaire sans armature Code : BVA011
- AVALUS, Bioprothèse valvulaire aortique avec armature Code : BVA012
- CARPENTIER-EDWARDS PERIMOUNT 2900, Bioprothèse valvulaire aortique avec armature Code : BVA013
- CARPENTIER-EDWARDS PERIMOUNT MAGNA EASE 3300TFX, Bioprothèse valvulaire aortique avec armature Code : BVA014
- INSPIRIS RESILIA 11500A, Bioprothèse valvulaire aortique avec armature Code : BVA015
- CARPENTIER-EDWARDS PERIMOUNT RSR 2800TFX, Bioprothèse valvulaire aortique avec armature Code : BVA016
Sous-section 2 : Bioprothèses valvulaires mitrales
- PERICARBON MORE MITRAL, Bioprothèse valvulaire mitrale avec armature Code : BVM001
- EPIC Mitrale, Bioprothèse valvulaire mitrale avec armature Code : BVM002
- HANCOCK II, Bioprothèse valvulaire mitrale avec armature Code : BVM003
- MOSAIC, Bioprothèse valvulaire mitrale avec armature Code : BVM004
- CARPENTIER-EDWARDS PERIMOUNT MAGNA MITRAL EASE 7300TFX, Bioprothèse valvulaire mitrale avec armature Code : BVM005
- CARPENTIER-EDWARDS PERIMOUNT PLUS 6900P Mitral, Bioprothèse valvulaire mitrale avec armature Code : BVM006
- CARPENTIER-EDWARDS PERIMOUNT PLUS 6900PTFX Mitral, Bioprothèse valvulaire mitrale avec armature Code : BVM007
Sous-section 3 : Bioprothèses valvulaires à position multiple
FREESTYLE, Bioprothèse valvulaire sans armature Code BVP001
Il est important de noter que depuis mai 2021 et la mise en application du règlement Européen (UE) 2017/745 relatif aux dispositifs médicaux, chaque dispositif médical de classe III doit avoir un code IUD. Les dispositifs médicaux de la liste intra GHS disposent donc d’un code IUD (Voir notre dossier sur les codes IUD).
Comment déclarer l’utilisation de ses dispositifs médicaux intra GHS ?

Les établissements de santé utilisant ce type de dispositif devront envoyer un fichier spécifique dans le cadre du PMSI et de la campagne tarifaire et budgétaire 2022.
Chaque mois les centres utilisateurs devront envoyer la liste des dispositifs à l’ATIH. Le code IUD-ID des dispositifs concernés servira de code pivot à l’ATIH.
La structure du fichier demandé est la suivante :
|
Libellé |
Nom variable |
Commentaires |
|
N° FINESS PMSI |
finesspmsi |
9 caractères |
|
Numéro administratif local de séjour |
numadmin |
|
|
ID Exp |
id_exp |
N9905 |
|
N°ordre |
id_ord |
1 |
|
Date d’utilisation |
date_util |
JJMMAAAA |
|
Code IUD-ID |
code_iud_id |
Défini à l’article 27 du règlement (UE) 2017/745 relatif aux dispositifs médicaux |
|
Nombre d'unités implantées |
nb_unitimpl |
|
A quelle date rentre en application la liste des dispositifs médicaux intra GHS ?
Le recueil est facultatif à partir de janvier 2022 et deviendra obligatoire à compter d’avril 2022.
Quelles différences entre un dispositifs inscrit sur la liste T2A et inscrit sur la liste Intra-GHS ?
Dans le cadre de leur prise en charge, les dispositifs médicaux peuvent être soumis à des évaluations complémentaires à celles relatives au marquage CE. Ces évaluations sont réalisées par la CNEDIMTS.
Deux procédures d'évaluation selon les modalités de prise en charge du dispositif médical sont prévues :
- via la LPPR : à l'initiative du fabricant ou du distributeur ;
- via les prestations d'hospitalisation : les catégories devant faire l'objet d'une évaluation sont définies par un arrêté ministériel.
|
Modalité de prise en charge demandée |
Liste des Produits et Prestations Remboursables (LPPR) |
Inclus dans le tarif des prestations hospitalières (INTRA-GHS) |
|
Champ des DM |
DM à usage individuel |
DM à appartenant à certaines catégories à évaluer, définies par arrêtés |
|
Secteur de prise en charge |
- Ville (LPPR) |
- Établissement de santé (INTRA-GHS) |
|
Type d’inscription |
- Nom marque |
- Nom marque |
Quel est le circuit pour l’inscription d’un dispositif médical sur la liste intra-GHS ?
L’industriel qui souhaite inscrire son dispositif médical sur la liste intra-GHS doit déposer une demande auprès du CNEDIMTS et conjointement auprès de la DGS et de la DSS. Le CNEDIMTS évalue l’efficacité clinique du dispositif ou son caractère spécifique ou son efficience par comparaison aux dispositifs déjà commercialisés. Pour connaitre les modalités complètes (et complexes) pour une inscription suivez ce lien.
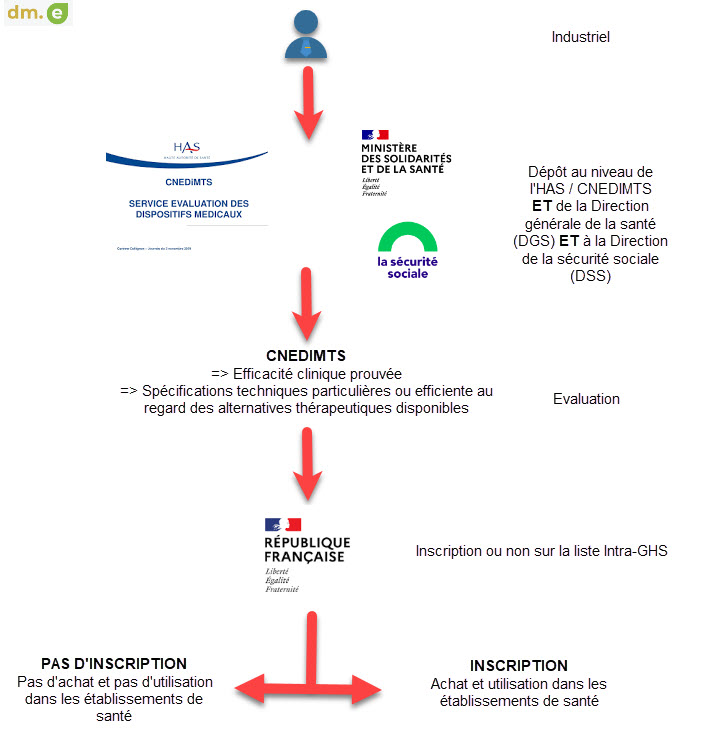
À la suite de son analyse, le CNEDIMTS demande ou non l’inscription du dispositif sur la liste intra-GHS. L’inscription se fait par arrêté et s’effectue en nom de marque ou en ligne générique.
Où retrouver de l’information sur les dispositifs médicaux intra-GHS ?
Exhausmed propose des monographies détaillées sur chacun des dispositifs médicaux inscrits sur la liste intra GHS. Ces monographies sont consultables depuis notre site DMPro ou directement dans les logiciels hospitaliers à l’aide de nos API. Pour connaitre nos solutions, n’hésitez pas à nous contacter ou à tester gratuitement notre base de données de dispositifs médicaux.
Comment vous pouvez nous contacter ?
- Par mail à info@exhausmed.com
- Par téléphone au 01 80 91 99 08
- Sur notre page contact : https://exhausmed.com/contact/
- Sur LinkedIn : https://www.linkedin.com/company/exhausmed/
- Par courrier :
EXHAUSMED
21 Rue Aristide Briand,
94100 Saint-Maur des Fossés
https://exhausmed.com/contact/
